
- 首页
- >
- GENESEED
- >
Lancet子刊丨生物信息学和计算生物学为环状RNA疫苗开发带来革命性突破
随着生物信息学与计算生物学的快速发展,环状RNA疫苗研发在序列优化、递送策略及药效学评估等关键环节迎来了革命性突破。近日,广州国家实验室于京佑/北京大学赵东宇等人团队在eBioMedicine期刊上发表综述:Unlocking the potential of circular RNA vaccines: a bioinformatics and computational biology perspective。

论文综述了生物信息学和计算生物学如何优化circRNA疫苗设计,阐明内部核糖体进入位点(IRES)的选择、开放阅读框架(ORF)优化、密码子使用、RNA二级结构预测和递送策略的发展,并提示利用计算机策略可以提高circRNA疫苗的生产效率和治疗效果,有利于推进circRNA疫苗的开发和应用。
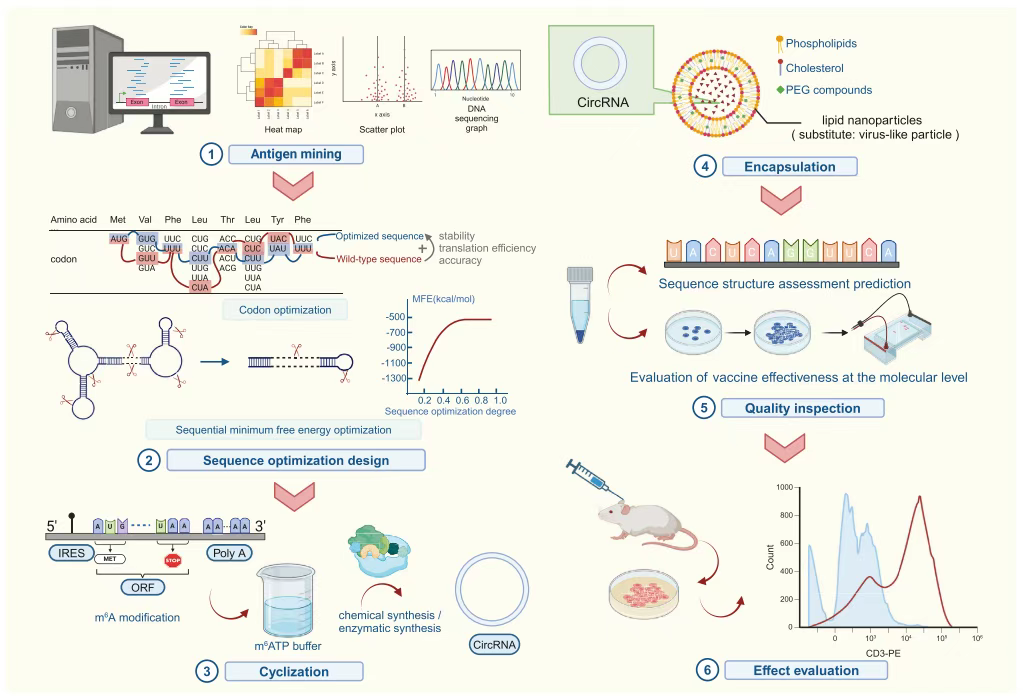
图1 设计和生产circRNA疫苗的工业化过程示意图。
一、候选circRNA的挖掘
生物信息学工具资源能够快速、有效地分析大规模数据,加速候选circRNA的鉴定,提高疫苗开发效率。
circRNA检测工具:CIRI2、circRNAprofiler、circtools、CIRCPlus、和CirComPara2等。
circRNA数据库:circBank、circBase、circAtlas、PlantCircNet、CircFunBase、CircRNADb、和AtCircDB等,收录了使用不同的鉴定工具和NGS数据集的文献中预测的circRNA。
二、ORF序列的选择和优化
免疫原性
circRNA疫苗的编码序列应优先考虑具有广泛免疫原性的病毒或蛋白质序列。组合文库对于识别表位模拟物和交叉反应序列很有价值。利用生物信息学工具可以预测免疫原性序列,降低人类白细胞抗原(HLAI)类分子的抗原肽亲和力。例如,BepiPred-2.0可预测B细胞表位,NetMHCpan4.0可识别T细胞表位和癌症新抗原;计算推断的HLA等位基因频率,评估疫苗的覆盖率,可确保其广泛的适用性。
密码子使用偏好性(CUB)
CUB在调节RNA蛋白质表达、稳定性、翻译效率和共翻译折叠中发挥关键作用。密码子优化基于丰富tRNA对应于高频密码子可以增加翻译效率的假设,通过用高频宿主密码子替换稀有密码子,重新设计核酸序列,而不改变编码的氨基酸序列,从而增强异源系统中的蛋白质表达。
测量mRNA衰变率等传统方法,可能会错过关键信息。而通过测量如tRNA适应指数的先进的指标,可以评估核糖体tRNA利用效率。量子计算、递归神经网络(RNN)和深度学习(DL)等计算机技术的进展,可优化设计序列在靶宿主生物体中有效表达。
针对mRNA的LinearDesign算法,在密码子优化或最小化自由能两个方向上进行联合优化,采用LinearDesign候选ORF的circDesign可对circRNA进行结构预测和序列设计,然后将其与IRES基序和其他功能区组装,评估位置熵和整体多样性以分析其对circRNA性能的影响。circDesign可以减轻ORF区域和IRES基序之间的相互作用,以实现功能性IRES的有效折叠;同时可防止circRNA的残留外显子片段对其他组分的折叠产生潜在干扰。
三、结构计算预测
二级结构预测
RNA二级结构计算方法,包括热力学、概率、和系统发育模型以及假设预测算法。mfold和RNAfold等被广泛使用的传统工具依赖于热力学参数和动态编程。然而,机器学习和深度学习的发展帮助开发更多复杂的工具,如MXfold2、UFold和SPOT-RNA,这些工具显着提高了预测准确性。cRNAsp12专门为circRNA设计,采用基于螺旋概况分区策略来预测最小自由能结构,并允许用户为精确预测施加结构约束。此外,Vienna RNA也适用于circRNA,可从内部和外部子结构有效计算环状结构,而无需显著的计算开销。
三级结构预测
IsRNAcirc等工具利用粗粒度分子动力学模拟在四步工作流程(输入准备、末端封闭、结构预测和模型优化)中,证明了优于基于模板的方法的优越性能。最初为线性RNA设计的3dRNA工具已适用于circRNA,揭示了一些circRNA表现出与其线性对应物相似的三级结构。
RNA-蛋白质复合物结构预测
预测工具包括RoseTTAFold 2NA和Alchemy_RNA2等。而AlphaFold3可以更准确地从结构生物学的角度预测蛋白质和核酸的复合物,可提供关于RNA分子的更多信息,并缩短疫苗设计周期。
四、IRES序列功能、机制和优化
circRNA可由IRES元件介导翻译,IRES元件具有相似的二级结构。高通量测定已验证了900多种IRES元件,而仅有一小部分circRNA(<1.5%)含有这些序列。许多IRES样元件富含AU,类似于聚腺苷酸化信号,但不会诱导circRNA降解。IRES介导的翻译效率因细胞环境而异,可根据应用进行灵活选择。
IRES数据库
IRESite为每个IRES补充了92种生物学方面的信息。IRESbase数据库从文献中注释了实验验证的最小功能的IRES元件,并总结了线性和环状RNA宿主的情况。IRESbase收录了1328条IRES,专注于中位长度为174nt的最小功能元件,以确保包含必要的序列,为研究人员探索circRNA机制和应用提供强大的资源,推动该领域的新发现和创新。
优化IRES序列长度
较长的circRNA意味着形成更大的二级结构并增加环化难度。因此,在设计序列时,应该优先选择较短的IRES样元件,例如Kozak序列和富含AU的序列。MHC-I类和II类配体的测序已经确定了新型抗原,为用免疫学有效的较短序列替代长ORF提供了理论基础。
RBP和miRNA调控
工程化RNA翻译调节通常涉及RNA结合蛋白(RBP)和miRNA,工程化circRNA可以在IRES-ORF的上游和下游掺入UTR样序列,以模拟RBP结合位点,提高翻译效率;如PROMITAR平台,可以设计miRNA响应性IRES元件,以控制单个RNA构建体中的翻译激活和抑制,为生物医学应用提供可编辑和精确的circRNA调控。
五、序列修饰
m6A修饰还可介导circRNA实现非帽依赖的翻译和调节翻译效率,特别是在应激条件下,减轻免疫应答并增强稳定性。核糖体分析、计算预测和质谱技术揭示了广泛的m6A驱动的circRNA翻译。
单条circRNA序列的RNA修饰位点的预测工具包括RAMPred和iRNA-3typeA等,但这些工具基于非单核苷酸分辨率数据,准确性有限。利用高分辨率数据的SRAMP、Gene2Vec和WHISTLE等工具,适用性仍然限于特定物种。而结合CNN和BiLSTM的新型circRNA m6A甲基化预测模型,可在不同组织和条件下具有稳健性能。
六、递送系统开发
circRNA疫苗的递送系统包括病毒载体、脂质纳米颗粒(LNP)、基于聚合物的纳米颗粒、基于外泌体的递送和基于肽的载体。
机器学习(ML)模型可用于优化病毒载体,如AAV衣壳特性,提高其有效性并减少开发时间和成本。人工智能引导的可电离脂质工程(AGILE)平台可以进一步加速用于LNP介导的mRNA递送的可电离脂质的开发,提供了脂质文库的有效设计、合成和评估。此外,生物信息学的最新进展,包括深度学习模型和分子动力学(MD)模拟,使从头设计具有复杂结构基序的功能性抗原表位成为可能,增强了中和抗体的诱导。
七、翻译效率和产量评估
circRNA疫苗的可翻译性可以在多个层面上进行检测,包括在其结构、蛋白质和细胞系层面。如AlphaLisa,VaxArray和Luminex等平台提供相对简单的多路复用功能,提高检测的灵敏度、精度、速度和吞吐量。VAX-seq是一种基于牛津纳米孔测序的简化质量控制方案,提供了从质粒准备到最终配方的所有生产阶段的全面mRNA质量评估,具有未来mRNA疫苗质量控制的应用潜力。
八、疫苗质量和免疫应答评估
单细胞转录组测序可以通过分析CD16+单核细胞、抗原呈递途径和CD4+/CD8+ T细胞活化的变化,评估对疫苗的动态免疫应答,使其适用于评估疫苗有效性,但需要特别关注circRNA疫苗的长期影响。联合蛋白组、转录组、基因组、表观组等多组学分析,研究免疫应答和染色质动力学,可建立稳态和免疫应激条件下的个体免疫谱,为疫苗效力评估提供参考。
九、总结
circRNA疫苗的巨大潜力将彻底改变疫苗开发格局。基于其独特性质,协同应用生物信息学和计算生物学为应对当前和未来的临床应用挑战提供了强有力的平台。随着研究的不断推进,circRNA疫苗从实验室到临床的转化无疑将有助于为各种疾病提供更有效和更容易获得的治疗选择。
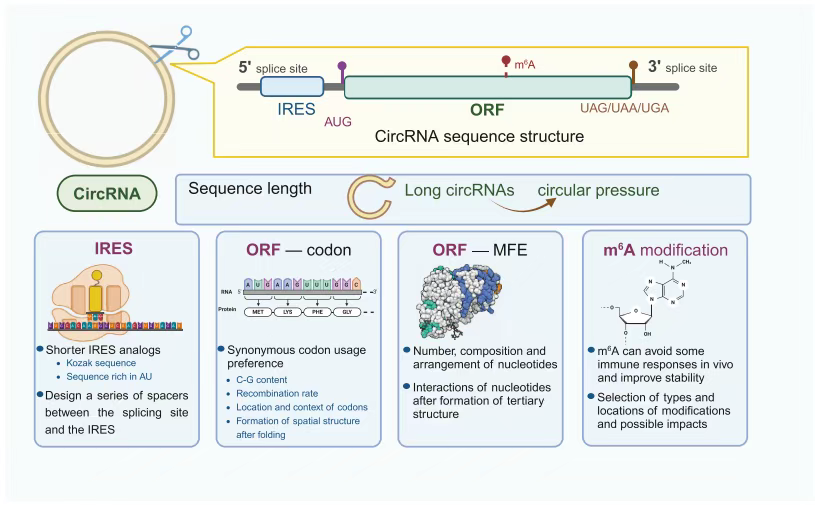
图2 通过生物信息学方法对编码抗原的ORF、IRES和两端的剪接位点等进行优化和重新设计,可显著提高疫苗的功效。
原文链接:
https://www.thelancet.com/journals/ebiom/article/PIIS2352-3964(25)00082-9/fulltext


 购物车
购物车


 广州市黄埔区开源大道11号科技企业加速器A区6栋2楼
广州市黄埔区开源大道11号科技企业加速器A区6栋2楼


 geneseed@geneseed.com.cn
geneseed@geneseed.com.cn