
- 首页
- >
- GENESEED
- >
如何从Polysome profiling入手,“拿捏”翻译研究?(含PLUS版攻略)
应激条件下,生物体如何快速调控基因表达?
病理情况下,致病蛋白如何过量表达?
胁迫环境下,全局基因表达如何重构生存策略?
如何验证预测潜在翻译RNA的翻译活性?
转录组和蛋白组变化水平为何不一致?
以上问题均可从RNA翻译的角度切入深究,我们之前已经介绍过各种翻译组分析技术,错过的朋友可以回头看看↓↓
推荐阅读:收藏!翻译组研究技术全览:Polysome/Ribo/RNC/Disome-seq
其中Polysome profiling被广泛应用于翻译研究。历久弥新的Polysome profiling还被称为翻译研究传统的“金标准”。[1]
Polysome profiling原理
翻译过程中,核糖体小亚基(40s)首先与mRNA的5’端结合,并沿5’→3’方向扫描mRNA,直到识别起始密码子。随后,60s核糖体大亚基在这个位置与40s亚基结合,形成具有催化活性的80s核糖体,进而启动肽链延伸及蛋白合成。由于多个核糖体可以同时结合同一条mRNA,因此mRNA上结合的核糖体数量可间接反映翻译活性。相比之下,仅结合单核糖体的RNA通常翻译水平较低或处于翻译停滞状态,而仅结合核糖体亚基的RNA可能尚未启动翻译。
Polysome profiling技术建立于20世纪60年代,根据核糖体结合RNA的翻译特性,结合越多核糖体的RNA沉降系数越大,基于蔗糖梯度超离心,可将细胞质RNA分离成无结合核糖体RNA(游离RNA)、结合40s和60s核糖体亚基、单核糖体(80s)和不同数量多聚核糖体等多个组分。通过分析RNA或蛋白质在不同组分的分布情况,可评估翻译状态,研究翻译调控机制。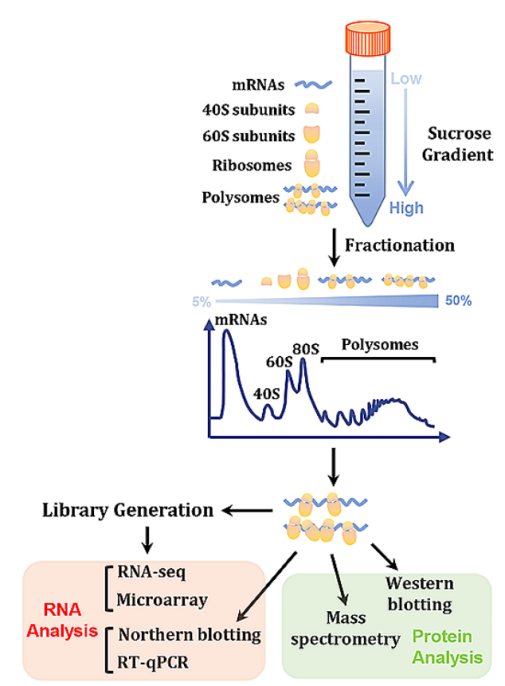
Polysome profiling技术路线图。[1]
Polysome profiling步骤
①裂解细胞:添加翻译延伸抑制剂,在增殖阶段裂解细胞,分离细胞质裂解液;
②超速离心:把裂解液转移到梯度蔗糖溶液后,超速离心将RNA分离成不同的组分;
③收集组分:利用密度梯度分馏系统,UV吸光度检测核酸浓度并收集各个组分;
④回收产物:从蔗糖溶液组分中回收RNA复合物;
⑤分析产物:绘制核糖体图谱;RT-qPCR分析特定RNA;高通量测序分析全局RNA概况;Western Blot或质谱分析蛋白质。
Polysome profiling技术优势
①高分辨率
Polysome profiling通过分离结合不同数量核糖体的RNA,可区分不同翻译活性的RNA,准确计算RNA的翻译效率(TE)。
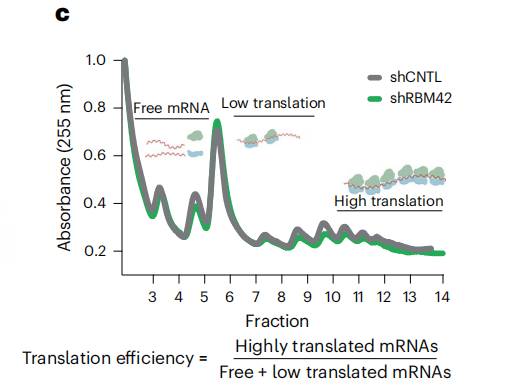
通过Polysome profiling计算TE。[2]
此外,Polysome profiling可作为Disome-seq等技术的预检测环节,查看图谱特定的峰,判断样本质量及是否适合下游检测。
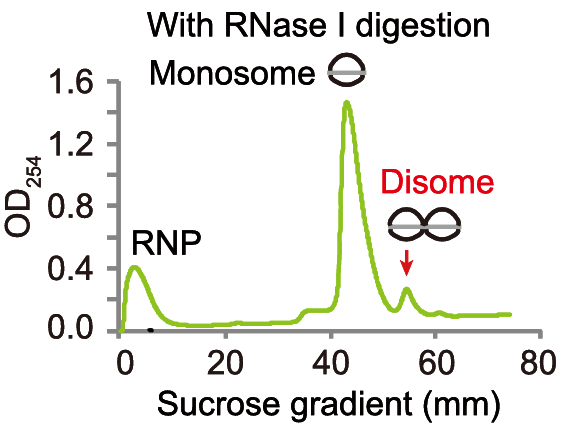
Polysome profiling中呈现双核糖体峰。[3]
② 动态监测
Polysome profiling体现RNA在各组分的分布变化,可捕捉药物处理、应激、病理等条件下的翻译活性的动态变化。
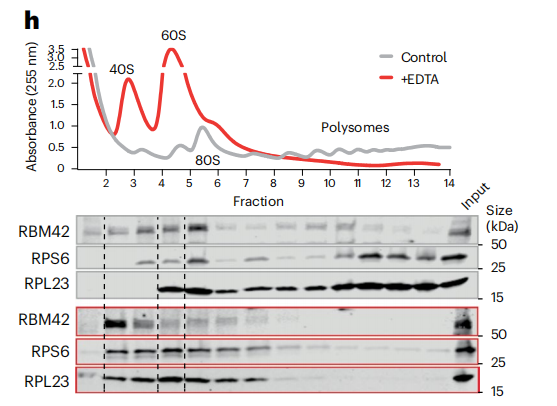
Polysome profiling分析EDTA处理和未处理的RNA翻译状态,同时研究翻译调控蛋白的分布。[4]
③ 高兼容性
Polysome profiling下游产物可进行多种检测:高通量测序分析全局翻译状态;RT-qPCR验证不同条件下特定基因的翻译状态;WB/质谱同步验证翻译活性,还可分析翻译调控因子。
④ 高灵活性
Polysome-seq可挖掘潜在翻译的ncRNA,并结合Polysome-qPCR验证翻译活性。从数据库或软件中预测到的潜在翻译ncRNA,也可以利用Polysome profiling+qPCR验证可翻译性,干湿实验结合,性价比更高!
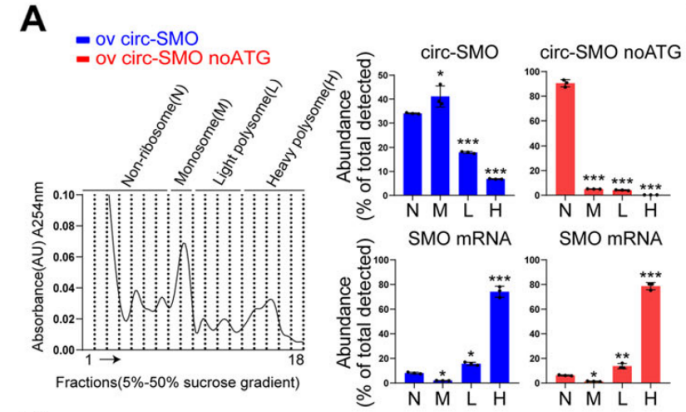
Polysome profiling验证胶质细胞瘤中circ-SMO的可翻译性。[5]
Polysome profiling难吗?不就是蔗糖溶液密度梯度离心吗?
对,但不全对!
① 需要专业设备:Polysome profiling需要用大型超速离心机,离心数小时以保证多个组分的清晰分离;随后的组分检测和收集也需专用的密度梯度分馏系统,包括流量控制的泵以及UV检测器。
② 操作较繁琐:需一系列繁琐的溶液配置、离心、分离、检测等操作步骤,耗时长且对操作者要求较高。
③ 容易受干扰:细胞内普遍存在高分子量的复合物,容易对多聚核糖体收集和检测造成干扰。
如何利用Polysome profiling出好结果?
①准备足够的样本
每个样本细胞量需≥ 1×107,且确保不同组别的样本细胞量一致。
②做好样本前处理
支原体检测:收集细胞样本(特别是用于测序的样本)做支原体检测,确保无支原体感染;
固定翻译状态:收集细胞前,细胞培养基中加入放线菌酮(cycloheximide),细菌样本需加入氯霉素(chloramphenicol)抑制翻译延伸;
收集细胞:对于贴壁细胞建议用胰酶消化,尽量避免用刮刀刮下细胞,而胰酶中也需加入放线菌酮。
私信公众号后台,发送“polysome”,可获取详细的Polysome profiling样本前处理详细步骤 。
③专业检测
一般实验室较少配备大型超速离心机,因此送专业的机构检测既可解决设备问题,又可解决繁琐且高难度的操作问题。
④合理选择组分
产物测序分析:用于评估全局翻译活性、筛选受翻译调控基因、筛选可翻译基因等。测序所需样本较多,成本较高。因此可以适当合并组分,一般选择一对组分用于对比,如结合多聚核糖体组分(P)vs 无结合多聚核糖体组分(NP)、结合多聚核糖体组分(P)vs无结合核糖体组分(ribosome-free)或结合多聚核糖体组分(P)vs总RNA等。
产物qPCR/WB检测:用于验证阶段,为准确评估RNA在各组分的分布变化,应尽量细分组分,获取足够的数据点,更准确地呈现特定RNA的翻译活性变化。

吉赛Polysome profiling plus

助力攻克各种翻译研究难题
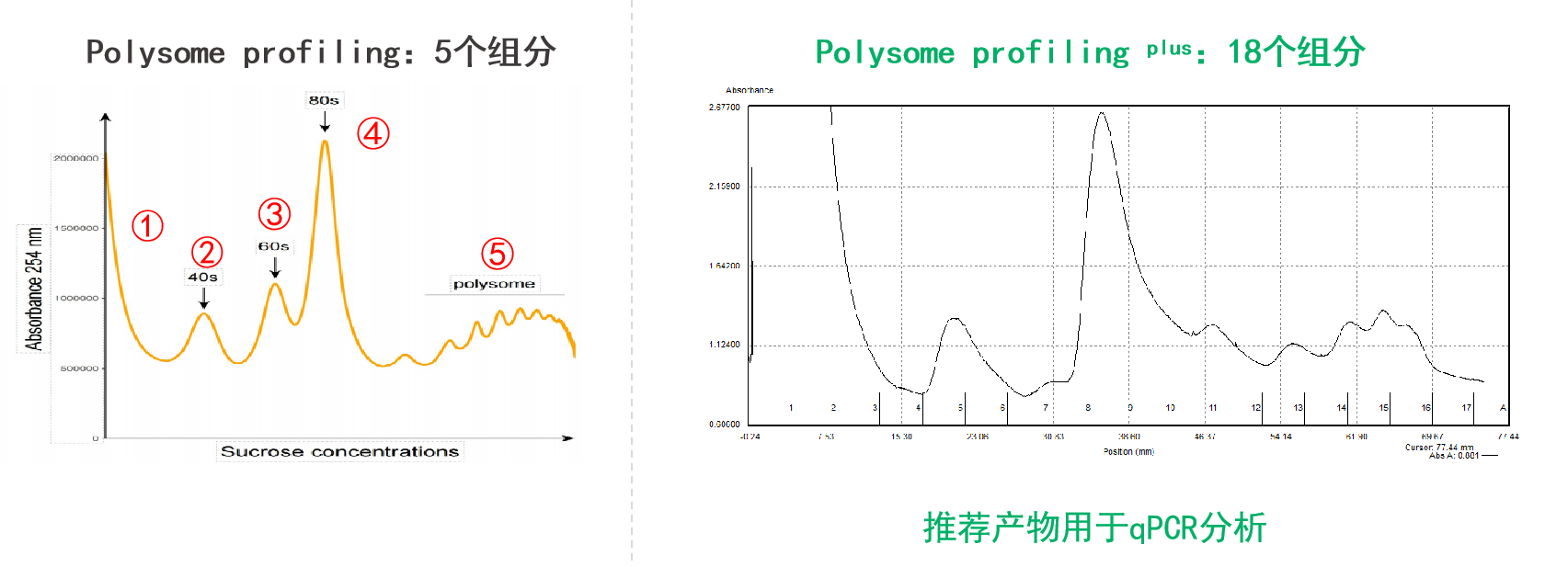
Polysome profiling plus升级内容:
①根据沉降系数大小,提供沉降系数从小到大共18个分离的组分,可增加RT-qPCR数据点,绘制更详细的翻译动态折线图,更精准反映翻译活性的动态变化;
②增加RNA质控,检测RNA完整性,确保下游的分析:
如送样不均衡,可根据质检结果进行相对等量上机(但不一定准,因为复合物含核酸和核糖体、蛋白等)
③能处理的样本类型增多:包括细胞、组织、细菌、真菌菌体等。
④统计AUC值(P/non-P ratio常用于表征样品整体的翻译活性)
例:
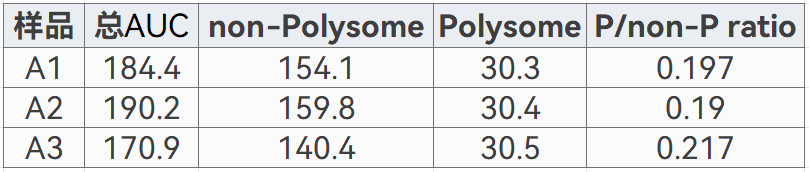
Polysome profiling 扩展包

参考资料
[1] Su D, et al. Ribosome profiling: a powerful tool in oncological research. Biomark Res. 2024, 12(1):11.
[2] Kovalski JR, et al. Functional screen identifies RBM42 as a mediator of oncogenic mRNA translation specificity. Nat Cell Biol. 2025 Mar;27(3):518-529.
[3] Zhao T, et al. Disome-seq reveals widespread ribosome collisions that promote cotranslational protein folding. Genome Biol. 2021 Jan 5;22(1):16.
[4] Kovalski JR, et al. Functional screen identifies RBM42 as a mediator of oncogenic mRNA translation specificity. Nat Cell Biol. 2025 Mar;27(3):518-529.
[5] Wu X, et al. A novel protein encoded by circular SMO RNA is essential for Hedgehog signaling activation and glioblastoma tumorigenicity. Genome Biol. 2021;22(1):33.

 购物车
购物车


 广州市黄埔区开源大道11号科技企业加速器A区6栋2楼
广州市黄埔区开源大道11号科技企业加速器A区6栋2楼


 geneseed@geneseed.com.cn
geneseed@geneseed.com.cn