
- 首页
- >
- GENESEED
- >
吉赛优选丨SomaScan ——体液蛋白组的“淘金利器”
体液做蛋白组没有想要的蛋白?
分析方法你用对了吗?
体液可以调节机体各个部位机能,同时也受多个部位状态影响。全面了解生理和病理状态下的体液蛋白组,可以促进分子标记和药物靶点的发现。体液是一条流动的“金沙河”,含有许多高研究价值的物质,但需要“淘金利器”。
体液蛋白组的动态范围极大,蛋白含量分布不均匀,含大量混淆视野的“泥沙”。在代表性体液——血浆中,有22种丰度达mg/mL的蛋白,占血浆总蛋白的99%,其中90%为白蛋白、免疫球蛋白和纤维蛋白原。血浆中还存在成千上万种有研究价值,但丰度极低(低至pg/mL)的蛋白质,如信号分子、炎症因子等。
蛋白组研究常用的质谱技术,容易受高丰度蛋白引起的压倒性“掩蔽”效应影响,导致仅表征丰度较高的蛋白,而忽略了大量丰度较低,但极具研究价值的蛋白。
开创性蛋白组研究技术:SomaScan
吉赛生物引入“淘金利器”——SomaLogic公司开发的SomaScan技术平台。吉赛生物拥有的SomaScan 7K/11K两大技术,通过一次上机可分别检测约7,000和11,000种蛋白,实现对体液蛋白质组,特别是低丰度蛋白质的全面和深入分析,加速生物标志物的发现和研究。
SomaScan技术原理
SomaScan是通过化学合成并修饰得到DNA适配体(Aptamer),筛选出针对目标蛋白特异性识别的适配体,将适配体进行标记得到SOAmer试剂。利用SOAmer特异性捕获目标蛋白质,然后对结合了蛋白质的DNA适配体进行DNA芯片或NGS检测,通过系统分析即可定性和定量分析样品的蛋白组。
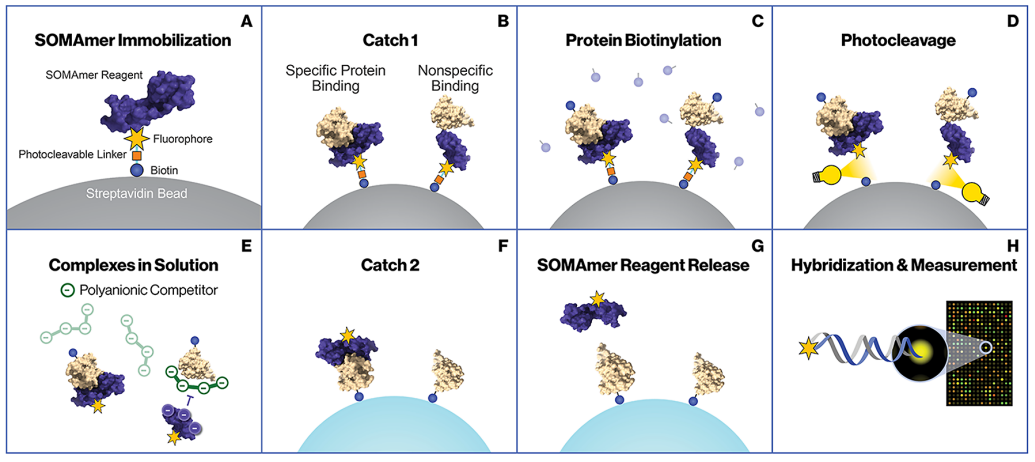
SomaScan检测流程[1]:
A:固化:SOMAmer的生物素结合链酶亲和素珠;
B:捕获:加入样品,SOMAmer结合蛋白,形成蛋白-SOMAmer复合物;
C:洗涤:洗涤去除未结合蛋白,结合的蛋白被生物素化;
D:释放:紫外光切割SOMAmer与生物素的连接区,SOMAmer-蛋白复合物释放到溶液中;
E:保护:光切割过程中,竞争性聚阴离子减弱非特异性蛋白再结合;
F:再固化:SOMAmer-蛋白通过蛋白上的生物素被捕获到链酶亲和素珠上;
G:提取:SOMAmer从蛋白复合物中解离;
H:检测:DNA芯片检测SOMAmer。
优势一:高覆盖度
SomaScan 11K最高可以在50μL血浆(建议用130μL)中,同时靶向检测11,000多种蛋白,即人类编码基因一半的蛋白量,其中包括10,000种人类特有的蛋白质,在血液中实际检出率90%。
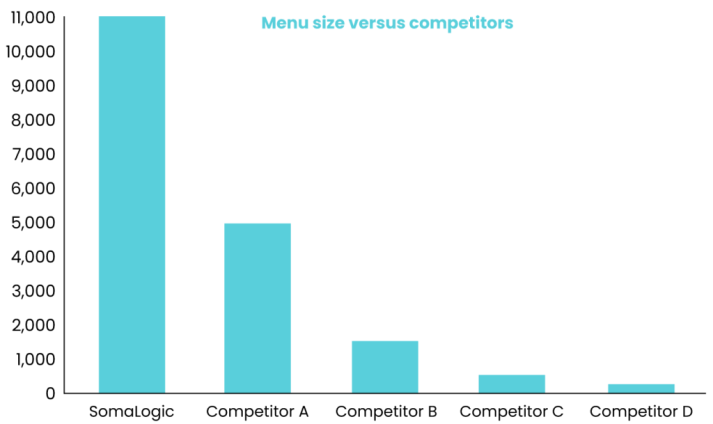
SomaScan的总蛋白质检测量是其它平台的两倍以上[2]
此外,SomaScan可检测所有主要生物通路中的蛋白质,全面挖掘有研究价值的蛋白,结合广泛性和靶向性,可确保蛋白质组学研究的深度和覆盖度。
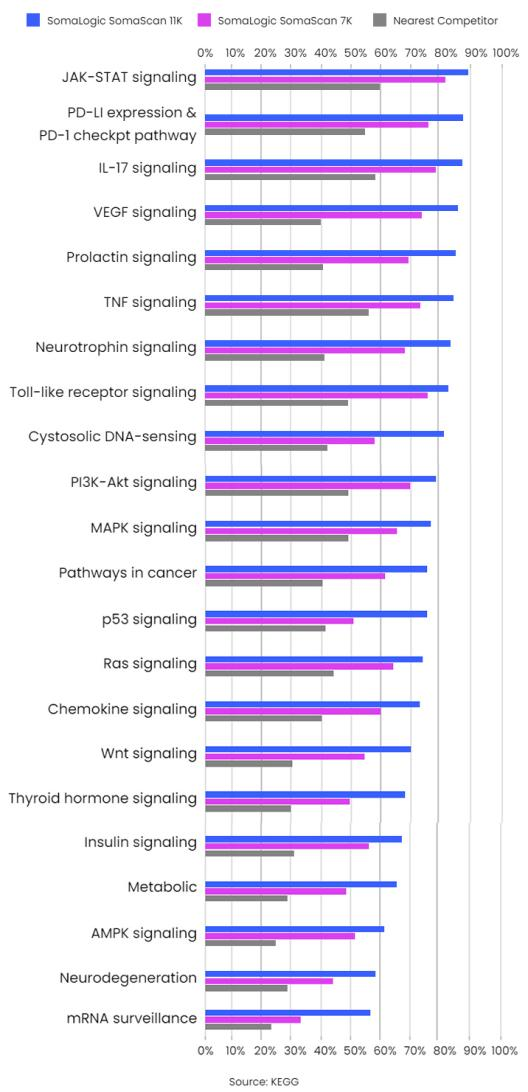
SomaScan平台在主要通路覆盖的基因占比[2]
优势二:高精准度
SomaScan采用独特修饰的特异性识别蛋白的单链DNA适配体技术,亲和力和特异性媲美抗体法,为FDA采用的唯一蛋白组鉴定方法。SomaScan检测精准度有赖于:
①利用动力学,使非特异性相互作用解离得更快,与相似蛋白质交叉反应极小;
②疏水性官能团修饰DNA,实现了更严谨的形状,可识别几乎相同的蛋白质;
③选择与目标蛋白结合严密的适配体,确保可经历严格的洗涤过程;
④利用竞争性聚阴离子,防止瞬态非特异性结合;
⑤避免了预设panel先入为主的偏见,更有利于发现新的生物标志物,提供对样品蛋白组新的见解。
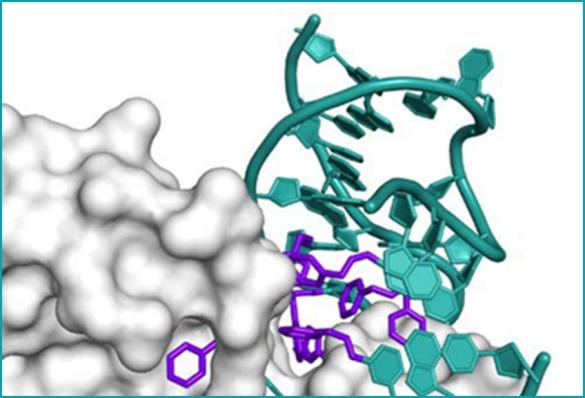
结合PDGF-BB的SOMAmer试剂的x射线晶体结构,紫色为碱基的修饰,蓝绿色为DNA适配体主干和未修饰的碱基[2]
优势三:高稳定性
SomaScan由于不依赖可变性高的多克隆抗体,其变异系数远低于行业标准(~5%CV),具有超高定量稳定性,避免了批次效应影响,可很好地应用于万人级别的队列研究中,以揭示极小的疾病状态和治疗效果变化,因而可应用于从靶点发现到药物开发整个管线的生物标志物检测。
优势四:灵敏度高
人血清/血浆中蛋白质的浓度上存在数量级的差异,大多数蛋白质组平台测量的蛋白质数量很少,动态范围较窄。SomaScan测量可采用连续稀释的方法,无需其它样品预处理,即可检测人血浆或血清中10-log动态范围内的蛋白(如从高峰度的白蛋白到低丰度的白细胞介素或干扰素),有利于发现罕见的蛋白质。
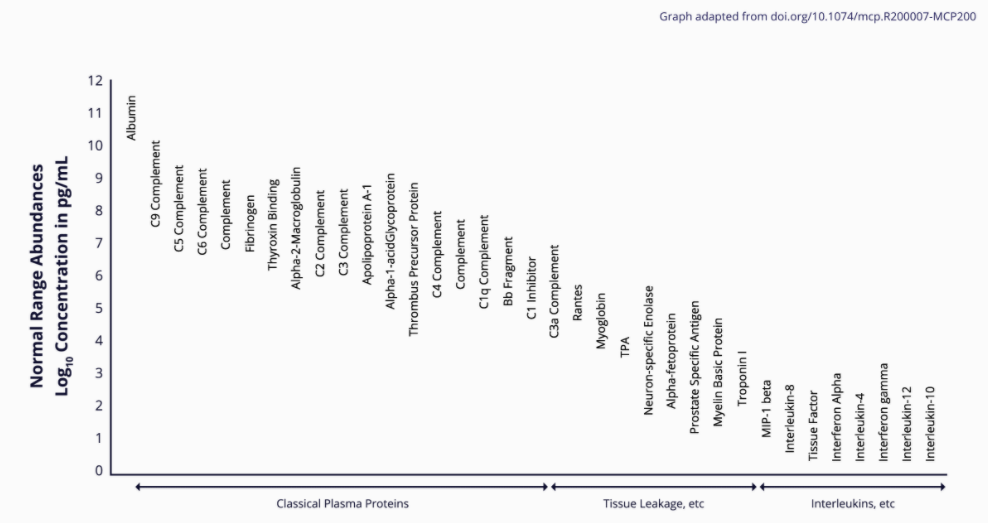
优势五:高灵活性
SomaScan平台可应用于多个物种(人、小鼠、大鼠、非人灵长类、猫、狗、猪等)和各种样品类型(血清、血浆、脑脊液、细胞裂解物、细胞匀浆等),不仅节省了时间和资源,而且便于无缝衔接动物模型和临床研究,以满足超大队列、临检、药检、科研等需求。
总之......
SomaScan可以高覆盖度、高灵敏度、高精准度、高稳定性、高灵活性地分析蛋白组,因而能无缝应用到科研生物标志物发现,药物研发药效分析,临床疾病进展或预后评估。
吉赛生物配备SmaScan技术平台,以及经验丰富的技术及分析人员,随时stand by,为广大科研人员从样本蛋白组中“淘”出高研究价值的蛋白。现在下单,还能赶上为国自然标书锦上添花哦~
案例分享
案例一:SomaScan筛选心力衰竭相关蛋白,建立风险评分模型
研究利用SomaScan技术平台分析了社区基础队列1,351名心力衰竭患者的7,289种血浆蛋白,筛选出38种标志性蛋白,建立蛋白质风险评分模型,用于心力衰竭患者的死亡风险评估,为未来的药物开发和治疗策略提供了重要的生物学信息。

蛋白质风险评分中39个SOMAmer(38种独特蛋白质)的Beta系数。[3]
案例二:SomaScan揭示慢性肾脏病心力衰竭的治疗靶点
研究利用SomaScan技术平台分析了2906名来自慢性肾功能不全(CRIC)者队列的4638种血浆蛋白,发现超过200种蛋白质与心力衰竭的发生显著相关,结合孟德尔随机化的算法,确定了6种可能直接影响心力衰竭发生的蛋白质,其中4种蛋白质是潜在的慢性肾脏病心力衰竭的治疗靶点。
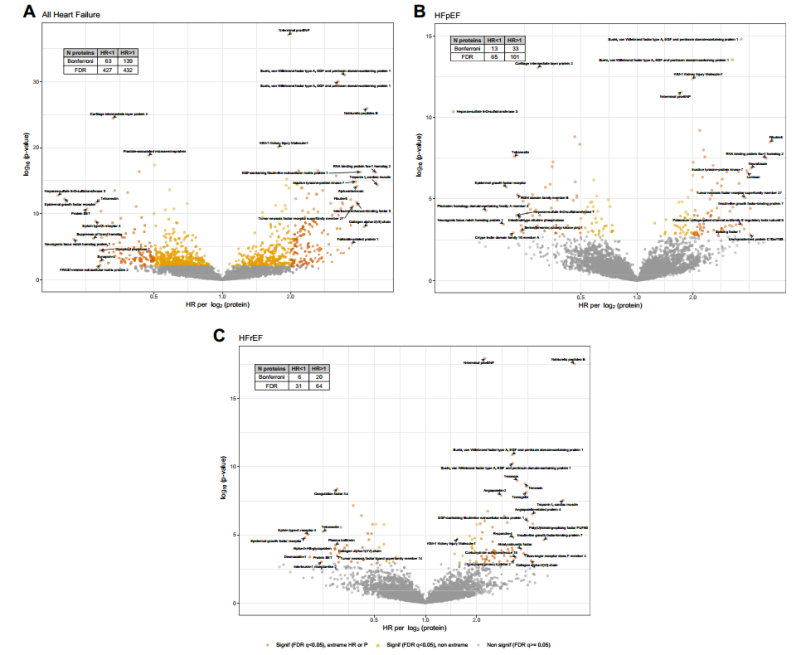
慢性肾功能不全患者中心衰相关的4638种蛋白火山图。[4]
案例三:SomaScan联合多组学深挖急性肾小管损伤生物标志物
研究利用SomaScan技术平台分析了434名肾脏疾病患者血浆样本,发现156种独特的血浆蛋白与急性肾小管损伤(ATI)显著相关;还结合区域转录组和蛋白质组、单细胞转录组测序(scRNA-seq)和通路分析,发现SPP1、MRC-1和TNC基因,以及相关的免疫调节和细胞器应激反应通路在ATI中具有重要作用。研究为未来针对ATI的药物开发和临床治疗提供了潜在的靶点。
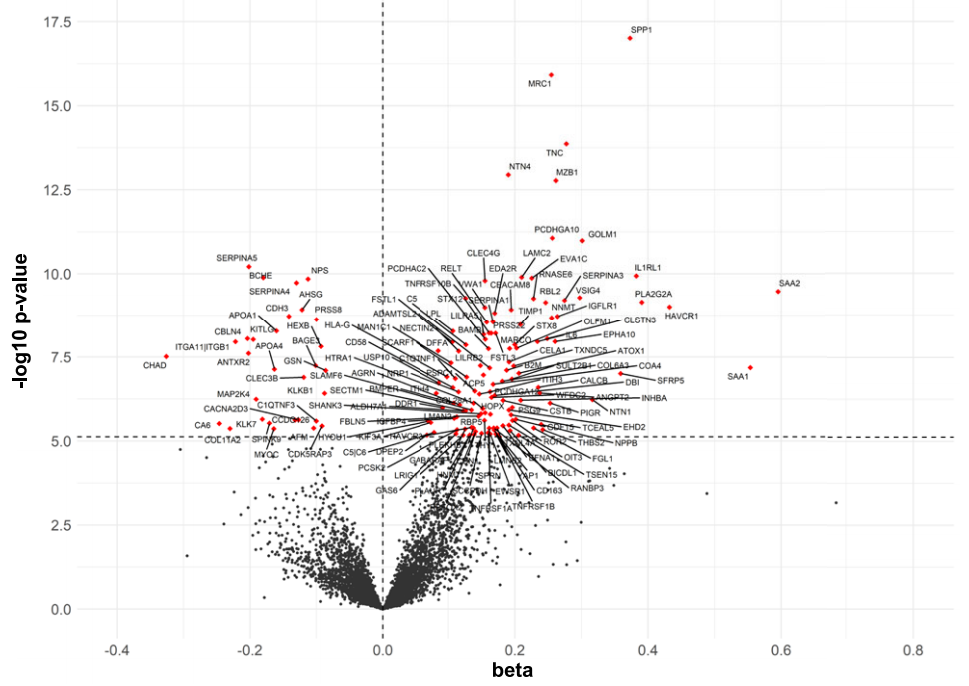
肾活检标本中与ATI严重程度相关的循环血浆蛋白。[5]
参考资料
[1]Kraemer S,et al.Crossing the Halfway Point:Aptamer-Based,Highly Multiplexed Assay for the Assessment of the Proteome.J Proteome Res.2024,23(11):4771-4788.
[2]https://somalogic.com/somascan-platform/
[3]Kuku KO,et al.Development and Validation of a Protein Risk Score for Mortality in Heart Failure:A Community Cohort Study.Ann Intern Med.2024,177(1):39-49.
[4]Dubin RF,et al.Incident heart failure in chronic kidney disease:proteomics informs biology and risk stratification.Eur Heart J.2024,45(30):2752-2767.
[5]Schmidt IM,et al.Plasma proteomics of acute tubular injury.Nat Commun.2024,15(1):7368.

 购物车
购物车


 广州市黄埔区开源大道11号科技企业加速器A区6栋2楼
广州市黄埔区开源大道11号科技企业加速器A区6栋2楼


 geneseed@geneseed.com.cn
geneseed@geneseed.com.cn